Cần thêm vào bao nhiêu ml dung dịch NaOH 0,25M vào 50 ml dung dịch hỗn hợp HCl 0,1M và H2SO4 0,05M để thu được dung dịch có pH =2 ?
A. 36,5 ml
B. 73ml
C. 22,4ml
D. 300ml
Cần thêm vào bao nhiêu ml dung dịch NaOH 0,25M vào 50 ml dung dịch hỗn hợp HCl 0,1M và H2SO4 0,05M để thu được dung dịch có pH =2 ?
A. 35,5 ml
B. 36,5 ml
C. 37,5 ml
D. 38,5 ml
1. Thể tích dung dịch NaOH 0,1M tối thiểu cần cho vào dung dịch hỗn hợp chứa 0,01 mol HCl và 0,02 mol AlCl3 để lượng kết tủa thu được là cực đại bằng?
2. *Cho 500 ml dung dịch Ba(OH)2 0,1M vào V ml dung dịch Al2(SO4)3 0,1M; sau khi các phản ứng kết thúc thu được 12,045 gam kết tủa Giá trị của V là?
3. Hoà tan hoàn toàn 47,4 gam phèn chua KAl(SO4)2.12H2O (K2SO4.Al2(SO4)3.24H2O) vào nước, thu được dung dịch X. Cho toàn bộ X tác dụng với 200 ml dung dịch Ba(OH)2 1M, sau phản ứng thu được m gam kết tủA. Giá trị của m là?
giải 3 bài trên theo pthh, ko dùng pt ion ạ
B1:
Cho dd NaOH vào hỗn hợp thì dd NaOH sẽ phản ứng với HCl trước sau đó mới phản ứng với muối AlCl3
Để kết tủa là cực đại <=> Không có quá trình hoà tan Al(OH)3
\(NaOH+HCl\rightarrow NaCl+H_2O\\ AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\\ n_{NaOH}=n_{HCl}+3.n_{AlCl_3}=0,01+0,02.3=0,07\left(mol\right)\\ \Rightarrow V_{ddNaOH}=\dfrac{n_{NaOH}}{C_{MddNaOH}}=\dfrac{0,07}{0,1}=0,7\left(lít\right)\)
2)
\(n_{Al_2\left(SO_4\right)_3}=0,0001.V\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,5.0,1=0,05\left(mol\right)\)
PTHH: \(3Ba\left(OH\right)_2+Al_2\left(SO_4\right)_3\rightarrow3BaSO_4+2Al\left(OH\right)_3\)
0,0003.V<--0,0001.V------>0,0003.V-->0,0002.V
\(2Al\left(OH\right)_3+Ba\left(OH\right)_2\rightarrow Ba\left(AlO_2\right)_2+4H_2O\)
(0,1-0,0006.V)<-(0,05-0,0003.V)
=> 233.0,0003.V + 78.(0,0008.V-0,1) = 12,045
=> V = 150 (ml)
3) \(n_{K_2SO_4.Al_2\left(SO_4\right)_3.24H_2O}=\dfrac{47,4}{948}=0,05\left(mol\right)\)
=> \(\left\{{}\begin{matrix}n_{K_2SO_4}=0,05\left(mol\right)\\n_{Al_2\left(SO_4\right)_3}=0,05\left(mol\right)\end{matrix}\right.\)
\(n_{Ba\left(OH\right)_2}=0,2.1=0,2\left(mol\right)\)
PTHH: \(3Ba\left(OH\right)_2+Al_2\left(SO_4\right)_3\rightarrow3BaSO_4+2Al\left(OH\right)_3\)
0,15<-------0,05----------->0,15----->0,1
\(Ba\left(OH\right)_2+K_2SO_4\rightarrow BaSO_4+2KOH\)
0,05---------------------->0,05--->0,1
\(KOH+Al\left(OH\right)_3\rightarrow KAlO_2+2H_2O\)
0,1--->0,1
=> mkt = mBaSO4 = 0,2.233 = 46,6(g)
\(n_{Ba\left(OH\right)_2}=0,5.0,1=0,05\left(mol\right)\\3Ba\left(OH\right)_2+Al_2\left(SO_4\right)_3\rightarrow3BaSO_4\downarrow+2Al\left(OH\right)_3\downarrow\\ \)
TH1: Nếu Al(OH)3 không bị hoà tan
\(\Rightarrow m_{kt}=m_{BaSO_4}+m_{Al\left(OH\right)_3}=233.0,05+78.\dfrac{2}{3}.0,05=14,25>10,045\left(loại\right)\)
TH2: Nếu Al(OH)3 bị hoà tan hoàn toàn.
\(2Al\left(OH\right)_3+Ba\left(OH\right)_2\rightarrow Ba\left(AlO_2\right)_2+4H_2O\)
=> \(m_{kt}=m_{BaSO_4}=233.0,05=11,65\left(g\right)< 12,045\left(g\right)\left(loại\right)\)
TH3: Kết tủa bị hoà tan 1 phần
Đặt:
\(n_{Al_2\left(SO_4\right)_3}=a\left(mol\right)\Rightarrow n_{Al^{3+}}=2a\left(mol\right);n_{SO_4^{2-}}=3a\left(mol\right)\\ n_{OH^-}=4.n_{Al^{3+}}-n_{\downarrow}\\ \Leftrightarrow0,1.2.0,5=4.2a-n_{\downarrow}\\ \Leftrightarrow n_{\downarrow}=8a-0,1\\ n_{BaSO_4}=3a\\ m_{\downarrow}=12,045\\ \Leftrightarrow\left(8a-0,1\right).78+3a.233=12,045\\ \Leftrightarrow a=0,015\left(mol\right)\\ \Rightarrow V_{ddAl_2\left(SO_4\right)_3}=\dfrac{0,015}{0,1}=0,15\left(lít\right)\\ \Rightarrow V=150\left(ml\right)\)
Hòa tan a gam FeSO4.7H2O trong nước, được 300 ml dung dịch A. Thêm H2SO4 vào 200 ml dung dịch A, dung dịch hỗn hợp này làm mất màu 30ml dung dịch KMnO4 0,1M. Vậy a có giá trị là:
A. 62,55g
B. 65,44g
C. 63,35g
D. 55,67g
Đáp án A
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Theo phương trình:
![]()
Trong 300ml có:
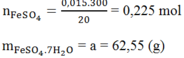
Chuẩn độ 20 ml dung dịch hỗn hợp HCl 0,1M + HNO3 a mol/l cần dùng hết 16,5 ml dung dịch hỗn hợp KOH 0,1M và Ba(OH)2 0,05M. Giá trị của a là:
A. 0,07
B. 0,08
C. 0,065
D. 0,068
Chuẩn độ 20 ml dung dịch hỗn hợp HCl 0,1M + HNO3 a mol/l cần dùng hết 16,5 ml dung dịch hỗn hợp KOH 0,1M và Ba(OH)2 0,05M. Giá trị của a là:
A. 0,07
B. 0,08
C. 0,065
D. 0,068
Hòa tan hết 10,4 gam hỗn hợp Fe, Mg vào 500 ml dung dịch hỗn hợp H2SO4 0,4M và HCl 0,8M, thu được dung dịch Y và 6,72 lít H2 (đktc). Cô cạn dung dịch Y thu được m gam muối khan. Giá trị của m là
A. 34,2≤ m ≤ 39,2.
B. 36,7.
C. 34,2.
D. 39,2.
Đáp án B
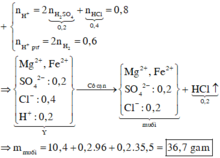
● Chú ý: Tiến hành cô cạn dung dịch chứa HCl, HNO3 thì các axit này sẽ bay hơi vì chúng có nhiệt độ sôi thấp.
Hòa tan hoàn toàn một lượng hỗn hợp Na và K vào nước được dung dịch A và V lít khí ở đktc. Để trung hòa hòa toàn dung dịch A phải dùng 75 ml dung dịch H2SO4 0,5M. Vậy V có giá trị là:
A. 0,56 lít
B. 0,672 lít
C. 0,84 lít
D. 1,12 lít
Đáp án C
Bài toán này có thể giải ngắn gọn như sau:
Số mol tạo ra = số mol H+ trung hòa = 2. Số mol H2
⇒ Số mol H2 = 0,075 : 2 = 0,00375 ⇒ V = 0,84 lít
Nhỏ từ từ tới hết V ml dung dịch HCl 1M vào 100ml dung dịch hỗn hợp Na2CO3 1M và KHCO3 2M. Sau phản ứng thu được dung dịch Y và 3,36 lít CO2 (đktc). Thêm Ba(OH)2 vào Y thu được kết tủa trắng. Tính giá trị của V
\(n_{CO_3^{2-}}=0,1\left(mol\right);n_{HCO_3^-}=0,2\left(mol\right);n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(CO_3^{2-}+H^+\text{→}HCO_3^-\)
0,1 0,1 0,1 (mol)
\(HCO_3^-+H^+\text{→}CO_2+H_2O\)
0,15 0,15 0,15 (mol)
Suy ra :
\(V=\dfrac{0,1+0,15}{1}=0,25\left(lít\right)\)
Cho hỗn hợp gồm 1,12 gam Fe và 1,92 gam Cu vào 400ml dung dịch chứa hỗn hợp gồm H2SO4 0,5M và NaNO3 0,2M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và khí NO (sản phẩm khử duy nhất). Cho V ml dung dịch NaOH 1M vào dung dịch X thì lượng kết tủa thu được là lớn nhất. Giá trị tối thiểu của V là:
A. 360
B. 240
C. 400
D. 120
Đáp án A
Số mol Fe = 0,02 mol; số mol Cu = 0,03 mol; số mol H+ = 0,4 mol;
số mol NO3- = 0,08 mol
Các phản ứng xảy ra:
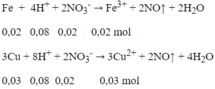
Sau 2 phản ứng trên, trong dung dịch X có 0,02 mol Fe3+; 0,03 mol Cu2+ và 0,24 mol H+ dư, ngoài ra còn có ion NO3- và SO42-. Tuy nhiên chỉ có 3 loai ion đầu là phản ứng với OH-.
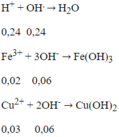
Tổng số mol OH- = 0,24 + 0,06 + 0,06 = 0,36 mol
→ V = 360ml